载亚硝基脲的多功能纳米载体的构建及其评价
DOI:10.13822/j.cnki.hxsj.2023.0264
背景介绍
卡莫司汀(BCNU)是临床上重要的抗肿瘤烷化剂,但由于肿瘤细胞内高表达的O6-烷基鸟嘌呤-DNA烷基转移酶(AGT)介导的耐药性,其抗癌效果被大大降低。临床上常将AGT抑制剂与BCNU联合使用来提高肿瘤细胞对抗癌药物的敏感性。然而,BCNU和AGT抑制剂均不具备肿瘤靶向性,往往导致药物对正常细胞的毒性增强,从而产生明显的毒副作用。因此,开发同时具备肿瘤细胞抑制能力、抗耐药活性和肿瘤靶向性的新型亚硝基脲类化合物,成为亟待解决的问题。纳米药物递送系统在改善药物水溶性、提高靶向性和降低毒副作用高等方面表现出巨大潜力,因此,本研究合成了一种叶酸修饰的抗耐药低氧激活纳米载体,用于BCNU的靶向递送。

文章亮点
内容介绍
1 实验部分
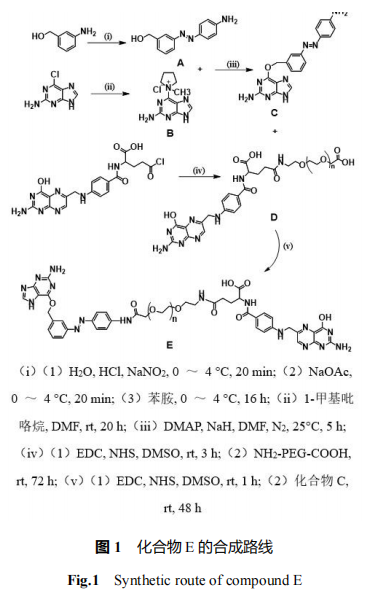
1.2.2 FA-PEG-AZO-BG/BCNU NPs的理化性质表征
2 结果与讨论
2.1 化合物D和E的结构表征

2.2 理化性质表征
2.2.1 粒径、形貌和稳定性表征
FA-PEG-AZO-BG NPs呈球形结构,纳米载体在H2O、PBS和含10% FBS的DMEM培养基中的粒径均无明显变化,说明FA-PEG-AZO-BG NPs具有较好的稳定性。

纳米载体可实现药物的有效包载,并且在不同投料比下,FA-PEG-AZO-BG/BCNU NPs对BCNU的包封率先上升后下降,载药量呈现逐渐上升的趋势,进一步观察发现,当投料比为2:10时,药物的包封率和载药量均较高,分别为59.56%和17.18%,故后续实验选用此药物投料比进行BCNU的包载。
3 结论



