
背景介绍
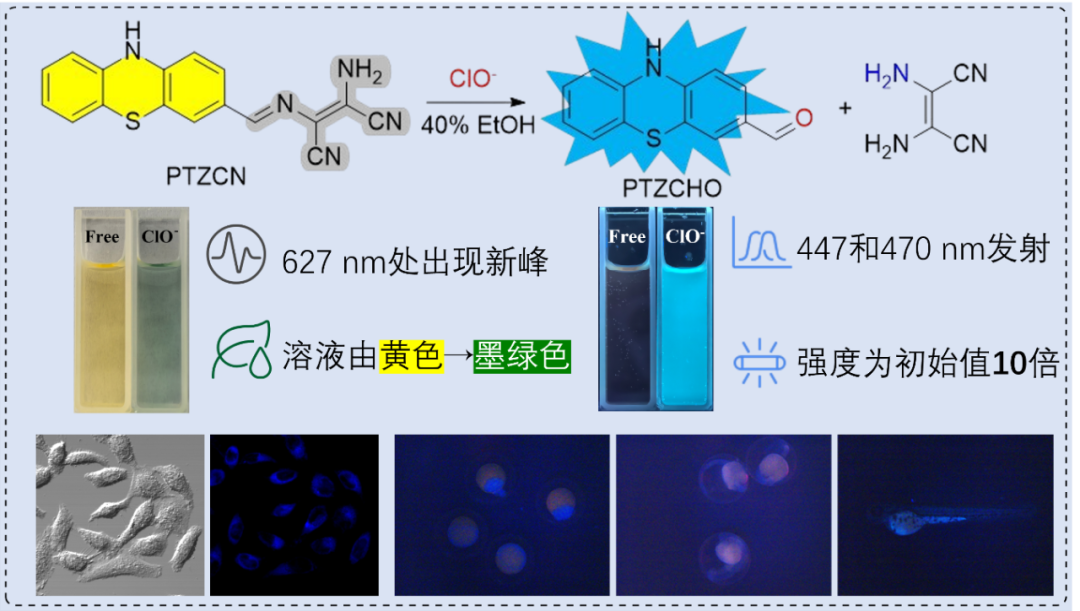
次氯酸(HClO/ClO⁻)作为关键活性氧物种,在免疫防御中具有重要生理功能。其在食品消毒领域被广泛应用,但因化学不稳定、易产毒副产物及体内瞬时存在,亟需发展高灵敏、实时检测方法。本文利用ClO⁻特异性诱导的C=N键氧化断裂机制,设计合成了一种新型吩噻嗪席夫碱衍生物PTZCN。该探针不仅展现出优异的灵敏度、宽pH适应性和良好选择性,更在宫颈癌细胞及斑马鱼模型中成功实现了次氯酸的实时检测与成像。
文章亮点
1. 基于ClO⁻特异性氧化C=N键断裂机制,合成了一种结构简洁、水溶性良好的吩噻嗪荧光探针分子;
2. 与ClO⁻作用后,该探针实现了吸收光谱从445 nm至627 nm的显著红移,并在447 nm处产生强蓝色荧光,检测限低至7.5 μmol/L;
3. 在细胞与活体层面实现ClO⁻精准检测,成功应用于HeLa细胞核定位成像及斑马鱼发育过程的时空分布监测。
内容介绍
1 实验部分
1.1 主要仪器与试剂
1.2 实验方法
1.2.1 探针PTZCN的制备
10-H-吩噻嗪-3-甲醛(PTZCHO)的按照文献[14]报道的方法制备。将1.135 g (5 mmol) PTZCHO和0.541 g (5 mmol)二氨基马来腈溶解于30 mL乙醇溶液中,滴加2滴冰醋酸,搅拌回流 12 h。反应完毕后将反应液倾倒入200 mL饱和食盐水中,用二氯甲烷萃取、无水Na2SO4干燥、减压浓缩后得粗产物。粗产物经硅胶柱层析(V(石油醚)∶V(乙酸乙酯)=5∶1)纯化得到棕色固体0.51 g,产率为32%。
1.2.2 溶液配制/测试方法
光谱测试:移取3.0 mL(2.0×10-5 mol/L)的PTZCN溶液(40%乙醇)于1 cm光程的石英比色皿中,加入30 μL(10-2 mol/L)的待测离子溶液,混合均匀后,立即进行紫外-可见吸收光谱和荧光发射光谱选择性测试。在选择性测试的样品中,再分别加入30 μL(10-2 mol/L)的ClO-溶液,进行光谱竞争测试。在探针溶液中,分别加入0~60 μL的ClO-溶液,进行光谱滴定测试。荧光光谱测定的激发波长为365 nm,灵敏度为中等,激发狭缝宽度为5 nm,发射狭缝宽度为3 nm。
2 结果与讨论
2.1 探针PTZCN对ClO-的光谱识别
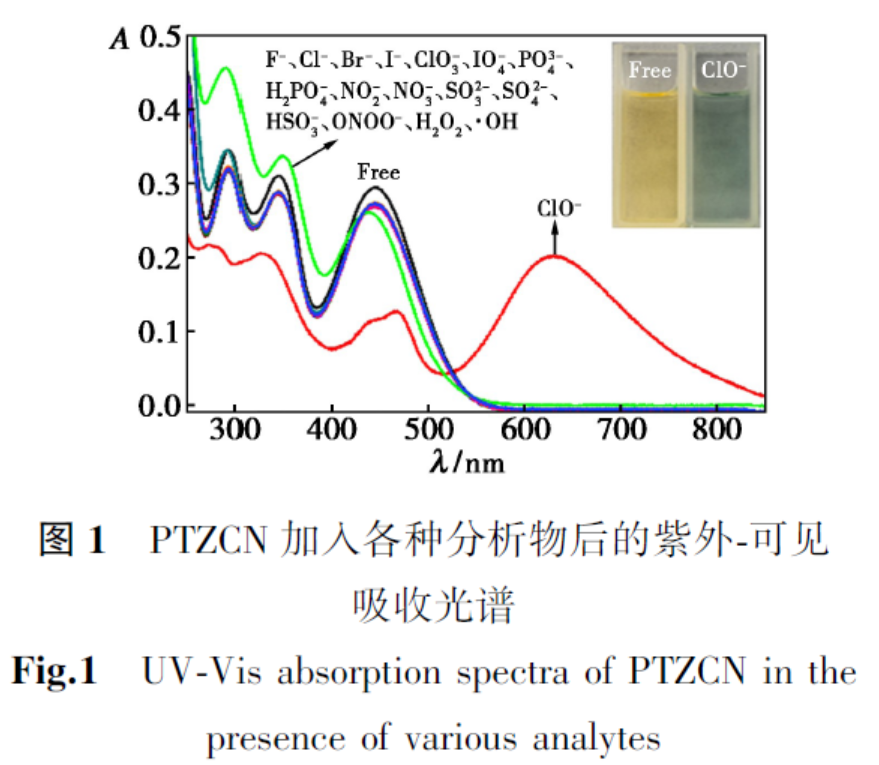
为了测试探针PTZCN对不同阴离子的特异性识别能力,在空白探针溶液(Free)中分别加入30 μL的待测离子或其他氧化性物种的溶液进行测试。如图1所示,大部分的待测物加入后,探针在293、344和445 nm处的吸收峰变化微弱;ONOO-加入后导致445 nm处的吸收峰出现了轻微的蓝移和减弱,紫外区的吸收出现了明显的增强(绿色线);而当向探针溶液中加入30 μL的ClO-后,627 nm处出现了新的吸收峰(红色线),293、344和445 nm处的吸收峰均出现了明显的降低,此时溶液的颜色由黄色迅速变为墨绿色。这可能是由于ClO-加入后,CN和吩噻嗪环上电子的π→π*跃迁过程被破坏,吩噻嗪的硫原子或芳香环向ClO-氧化生成的中间体转移电子,生成了电荷转移复合物。
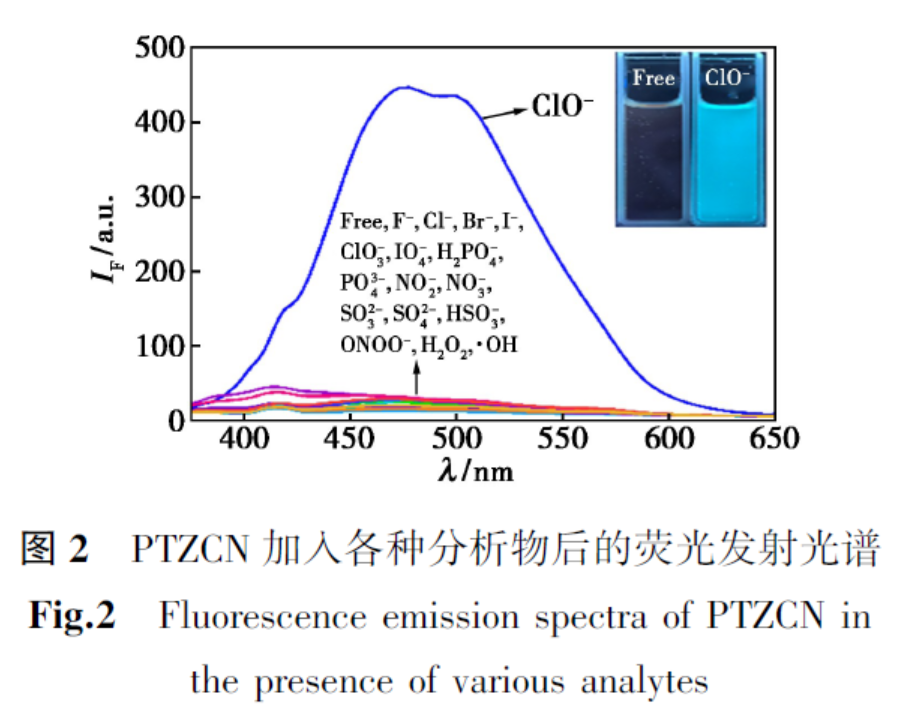
对探针分子进行荧光光谱选择性测试时(图2),发现加入的大部分阴离子和氧化性物种对PTZCN溶液的无明显荧光开启变化;而加入ClO-后,探针溶液在474和500 nm处出现明显的蓝色荧光发射,且强度为初始值的10倍以上。该结果表明,探针PTZCN对ClO-具有较好的荧光选择性。
2.2 探针PTZCN对ClO-的竞争实验
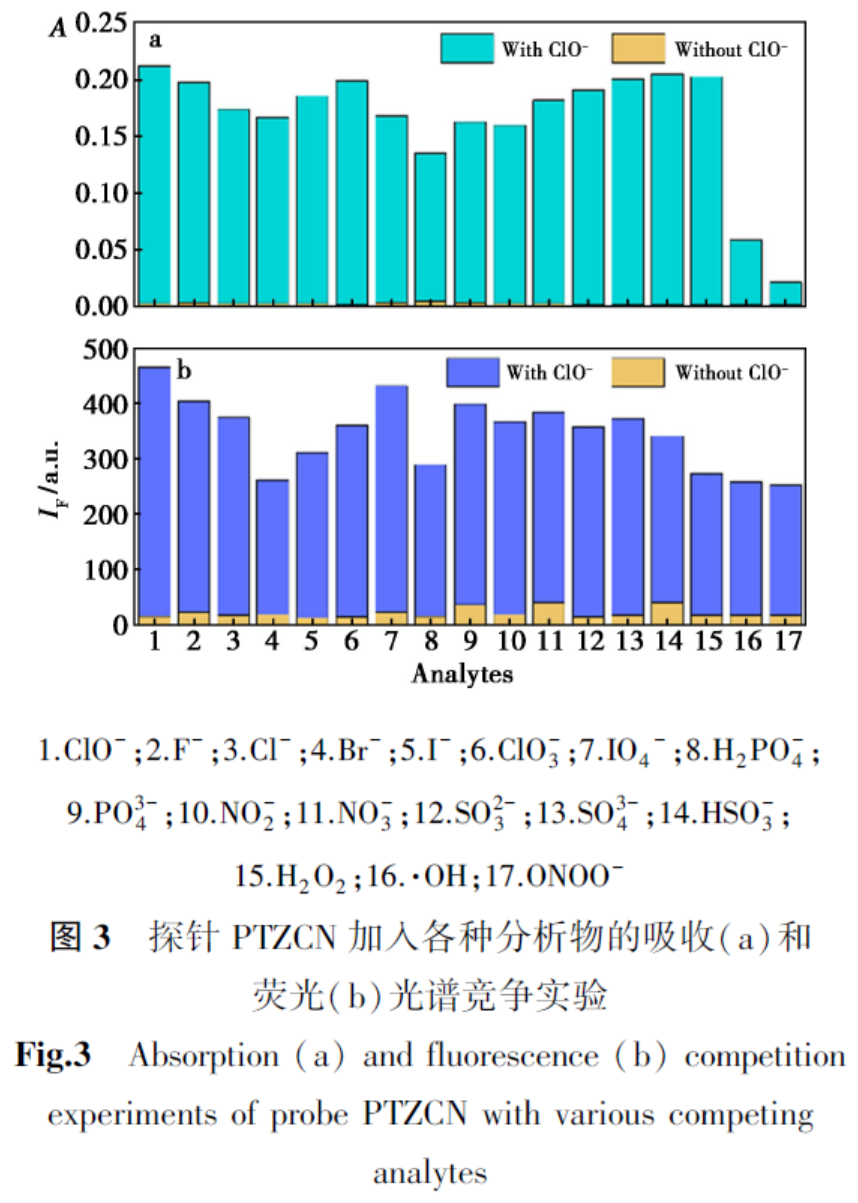
为了验证探针在复杂体系中对ClO-的识别能力,在两种离子共存的条件下,对其进行了竞争测试。从图3a可知,当待测液中无ClO-时,探针PTZCN在627 nm处的吸光度几乎为0;当向共存离子中加入ClO-后,除了活性较强的·OH和ONOO-外,大部分共存溶液的吸收强度均能出现大幅度上升,这可能是由于二者与ClO-在溶液中发生氧化还原反应,消耗了大部分的ClO-所致。当干扰分析物存在时,探针PTZCN的荧光强度均小于50;当ClO-加入后,共存溶液的荧光强度均迅速升高(图3b)。尽管活性较强的·OH和ONOO-消耗了加入的大部分ClO-,PTZCN仍能产生显著荧光增强,说明其对ClO-的反应能力优于其他活性物种。尽管在较高浓度的多种共存体系中观察到上述干扰现象,但在实际的生物环境中,由于上述干扰物的内源性浓度极低,潜在干扰通常不会发生。
2.3 探针PTZCN的光谱滴定实验
2.4 PTZCN在不同pH下对ClO-的响应
2.5 PTZCN识别ClO-的机理
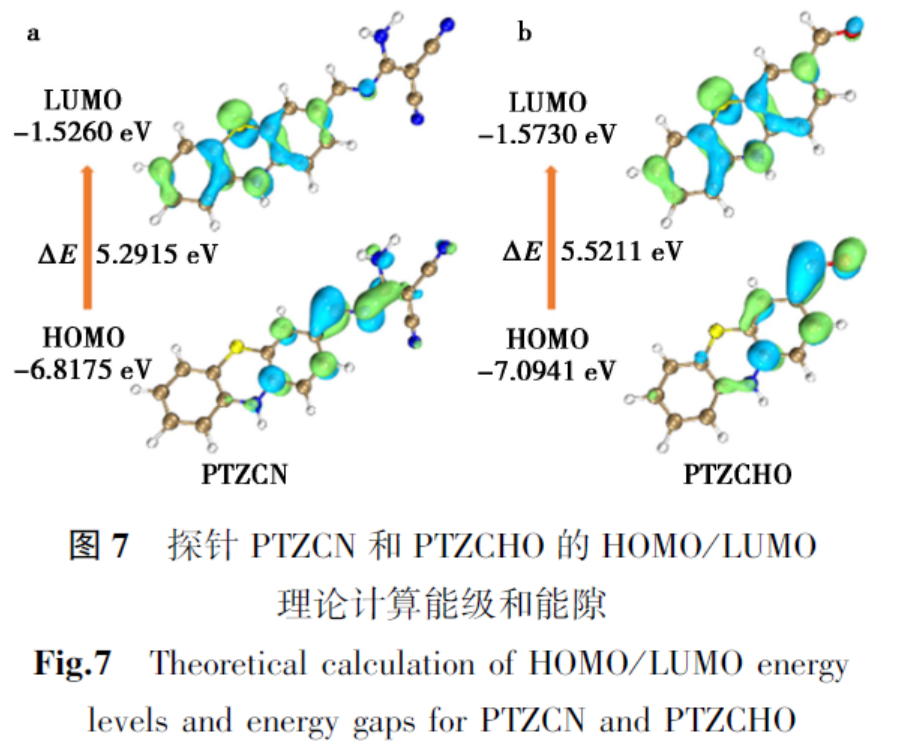
为了深入了解探针识别ClO-的过程,对探针进行了密度泛函理论(DFT)计算和ESI-MS测试。DFT计算显示,PTZCN的HOMO上的电子云主要分布在吩噻嗪分子上,而LUMO上的电子则都位于二氨基马来腈和CN键附近。这说明探针分子本身具有明显的电荷转移效应(ICT),激发态电子会从吩噻嗪向二氨基马来腈转移(图7)。当HClO氧化CN后,尽管LUMO依然位于吩噻嗪区域,但HOMO的电子云扩展范围受限,ICT过程被削弱。这种从PTZCN到PTZCHO的能级变化表明非辐射跃迁被抑制,荧光发射增强。ESI-MS测试发现,PTZCN的分子碎片峰m/z=317.073 5;与ClO-发生反应后,溶液中出现了新的碎片峰m/z=227.040 5,该峰与吩噻嗪醛PTZ-CHO相吻合。
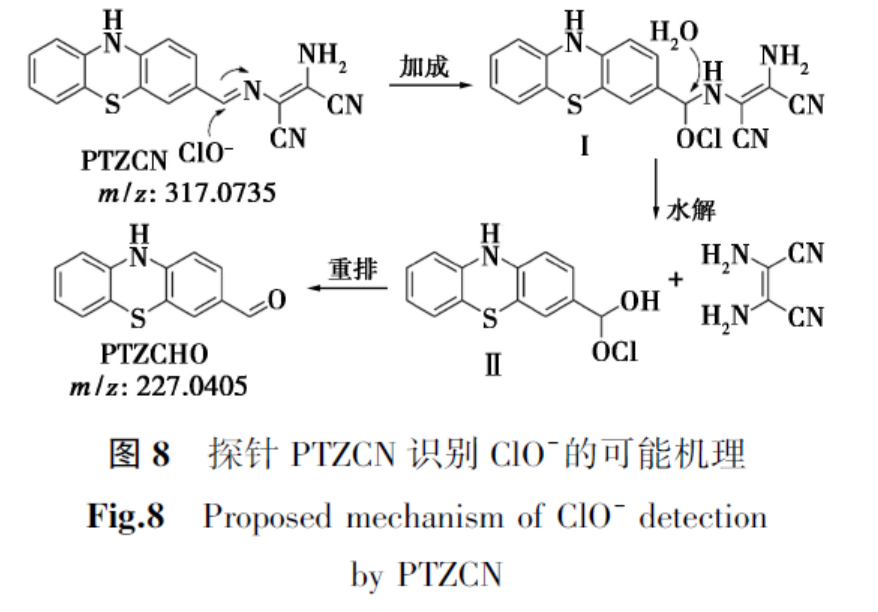
根据文献报道的反应机制[16,17],PTZCN识别ClO-的机理可能为:在水溶液中,探针分子CN键上的碳原子首先受到ClO-的亲核进攻,然后N原子接受H+质子,形成中间体I;随后I发生水解反应,生成不稳定的中间产物II;最终进一步重排形成吩噻嗪醛PTZCHO(图8)。
2.6 PTZCN在荧光成像中的应用
基于PTZCN对ClO-优异的传感性能,进一步评估了其在HeLa细胞中外源性ClO-成像的实际效果。如图9所示,仅与PTZCN(10.0 μmol/L)共孵育的HeLa细胞几乎未显示荧光信号(A1);相反,当细胞与探针PTZCN(10.0 μmol/L)及ClO-(100.0 μmol/L)共孵育后,则表现出强烈的蓝色荧光(B1);将明场和蓝光通道下的图片叠加,发现蓝色荧光主要分布在HeLa细胞的细胞核区域,而细胞质区无明显荧光变化。这表明探针PTZCN的特异性较高,可以用于荧光标记细胞核及对活细胞外源性的ClO-进行成像。

3 总结与展望
本文将吩噻嗪作为荧光团与二氨基马来腈通过缩合反应,制备了一种席夫碱类荧光探针分子PTZCN。
3.1 该探针在40%乙醇溶液中与ClO-反应形成电荷转移复合物,导致吸收峰红移(445→627 nm),并在470和500 nm处出现特征荧光发射。与文献报道的同类探针相比,其检测限已经达到微摩尔水平(7.5×10-6 mol/L),且在较宽的pH范围内对ClO-进行快速检测。
3.2 探针PTZCN在HeLa细胞中可实现外源性ClO-的特异性核定位成像,并在斑马鱼胚胎发育过程中呈现卵黄囊富集及72 h后头体部弱荧光分布的时空特征。
3.3 研究证实—CN和CN键作为ClO-特异性反应位点可显著提升探针氧化敏感性,为开发用于生物活体内次氯酸及其盐的生物成像材料提供可参考的策略。
通讯作者介绍

杨杨
个人简介
内蒙古民族大学化学与材料学院副教授,硕士生导师。曾先后承担国家自然科学基金项目、内蒙古自治区自然科学项目、内蒙古高等学校研究课题等6项。在Chem. Commun.、Chem. Eur. J、Sensors & Actuators B、Talanta、Spectrochimica Acta Part A等学术期刊上发表SCI论文20篇,发表CSCD核心论文6篇,授权国家发明专利2项,出版学术专著1部。
主要研究方向
有机荧光传感的设计与合成
近五年代表作
Spectrochimica Acta Part A, 2021, 248: 119238
Inorg. Chem., 2025, 64, 2496−2507
Spectrochimica Acta Part A, 2025, 332: 125815
Spectrochimica Acta Part A , 2026, 346: 126892
化学试剂,2020,42(08):987-991.
化学试剂,2025,47(12):77-82.



