手性螺环氧化吲哚类化合物的设计、合成及抗肿瘤活性研究
引用本文:张文会,郝知风,李凯,等.手性螺环氧化吲哚类化合物的设计、合成及抗肿瘤活性研究[J].化学试剂,2024,46(2):39-46.
DOI:10.13822/j.cnki.hxsj.2023.0569
背景介绍
螺环氧化吲哚骨架是许多药物、天然产物的基本结构,已有研究证实大部分此类化合物具有抗肿瘤活性,尤其结构中的手性季碳中心对螺环氧化吲哚类化合物的抗癌效果具有重要影响。因此,螺环氧化吲哚类衍生物的手性合成及抗肿瘤作用研究受到新药研发和合成人员的广泛关注。针对课题组前期利用优势骨架拼合原理,通过不对称串联Michael加成反应合成的27个手性螺环氧化吲哚-环丙烷-茚二酮类化合物,在分析其抗肿瘤活性与结构关系的基础上,进一步优化目标分子结构,以期得到抗癌活性更强的抗肿瘤候选有机分子。
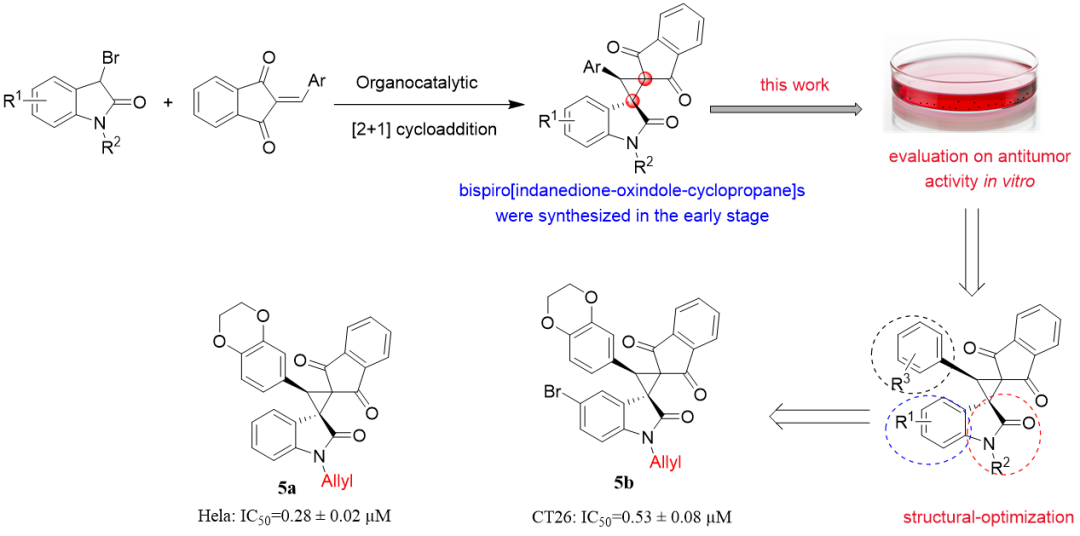
文章亮点
1.研究了27个手性螺环氧化吲哚-环丙烷-茚二酮类化合物的抗肿瘤活性;
2.根据构效关系分析,设计并合成了4个目标分子,研究显示其能有效抑制CT26和Hela细胞的增值;
3.部分手性螺环氧化吲哚类目标化合物可作为抗肿瘤药物候选先导化合物,具有较好的研发潜力。
内容介绍
1 实验部分
1.1 主要仪器与试剂
1.2 实验方法
1.2.1 手性螺环氧化吲哚类化合物的体外抗肿瘤活性研究
螺环氧化吲哚类化合物用DMSO溶解,并于-20 ℃保存。使用时常温解冻,并利用完全培养基稀释到所需浓度。通过数据分析软件计算抑制一半肿瘤细胞增殖的化合物浓度(IC50),以初步衡量化合物对相应肿瘤细胞的活性大小。
1.2.2 高活性苗头化合物的结构优化
经分析,保留原有整体骨架不变,将抗肿瘤活性较好的三个有效片段进行整合,得到二次优化的目标化合物5a、5b和5c(图3)。
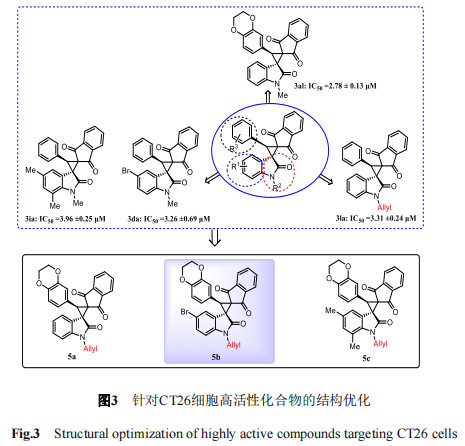
通过构效分析,选出具有代表性的化合物3ba、3ja及3aj,同样保持原有手性螺环氧化吲哚整体骨架不变的基础上,将抗肿瘤活性较好的取代基进行组合,设计得到结构优化的目标化合物6(图4)。
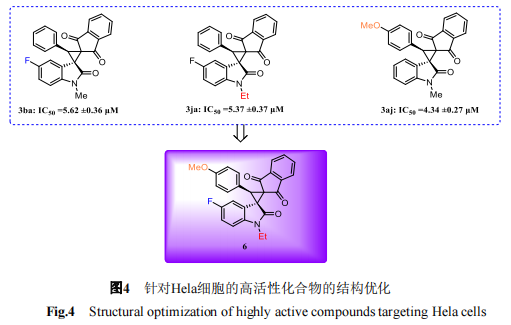
1.2.3 目标化合物的合成
目标化合物5a~5c及6的合成路线如图5所示。
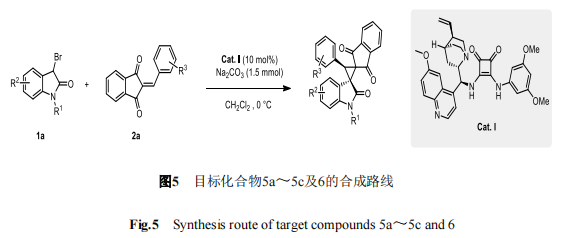
1.2.4 目标化合物5a~5c及6的抗肿瘤活性研究
为了探索其抗肿瘤活性是否提高,再次通过CT26和Hela肿瘤细胞模型,研究二次优化目标化合物的抗肿瘤活性。
1.2.5 分子对接
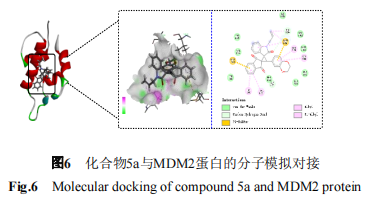
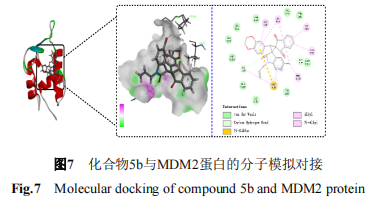
通过ligand interactions 模块分析其相互作用情况,结果见图6和图7。
2 结果与讨论
2.1 手性螺环氧化吲哚类化合物抗肿瘤初步构-效关系探析
根据手性螺环氧化吲哚骨架衍生物的结构及其体外抑制CT26及Hela细胞增值活性,得到化合物的抗肿瘤结构-活性关系初步为:
(1)构建的手性螺环氧化吲哚-环丙烷-茚二酮结构是发挥化合物抗肿瘤作用的有效骨架,这与文献报道的螺环氧化吲哚被称为诸多天然或合成药物的“特效支架”,在抗肿瘤药物候选化合物研发中具有重要研究价值一致[28,29];
(2)目标分子中,氧化吲哚和2-亚芳基-1,3-茚二酮骨架中的取代基对化合物的抗肿瘤活性有一定影响,特别对CT26细胞较显著,但规律性不明显。
2.2 高活性化合物结构优化及其抗肿瘤活性研究
通过有效片段组合得到的化合物5a及5b对CT26细胞和化合物6对Hela细胞的细胞毒性均比优化前强,推测螺环氧化吲哚骨架中吲哚芳环上引入吸电子效应的基团有利于抗肿瘤活性的提高。
2.3 分子模拟对接分析
根据对接结果推测合成的手性螺环氧化吲哚类化合物对CT26和Hela细胞的抗肿瘤作用机制与p53-MDM2途径有关,即化合物在肿瘤细胞中通过竞争性与MDM2蛋白结合,从而释放p53,激活p53信号通路以发挥其抗肿瘤作用,具体有待进一步试验验证。
3 结论
通过对前期合成的27个手性螺环氧化吲哚类化合物进行抗肿瘤活性研究,经构效关系分析,在保持原本结构基础上对抗肿瘤活性较好的基团或片段进行重组,得到二次优化的化合物5a对结肠癌CT26和宫颈癌Hela细胞均表现出较强的抗肿瘤活性,化合物5b对CT26细胞具有较好的抗肿瘤作用。通过分子对接,化合物5a和5b均能与MDM2蛋白有效结合,猜测其抗肿瘤途径可能与p53-MDM2信号通路有关。
总的来说,化合物5a及5b有望成为抗肿瘤先导化合物,后续将对其成药性及体内外抗肿瘤具体作用机制进行深入研究,以期发现高效、低毒的手性螺环氧化吲哚类抗肿瘤药物候选化合物,为此类抗肿瘤药物研发提供物质基础,以为其他活性先导化合物的发现提供参考和借鉴。



